Kita pasti tidak asing lagi
dengan reaksi redoks, dimana ada reaksi reduksi dan ada pula yang oksidasi. Nah
pada blog sebelumnya kita telah membahas mekanisme oksidasi pada berbagai
senyawa organik, dan sekarang pada pembahasan kali ini kita akan membahas tentang
mekanisme reaksi reduksi pada berbagai senyawa organik. Reduksi umumnya adalah
reaksi dimana elektron ditambahkan ke suatu senyawa. Senyawa yang mendapatkan
elektron dikatakan berkurang.
Adehid
dan keton
Aldehid
dan keton bisa direduksi jadi tiga (3) macam :
Ø Hidrokarbon
Ada Tiga macam metoda yang dapat
menjadi hidrokarbon yang berasal dari aldehid dan keton :
·
Metode
Wolff-Kishner
·
Metode
Mozingo
·
Metode
Clemmensen
Baiklah
yang pertama itu metode Wolff-Kishner dimana pada metode ini mengubah gugus fungsional
karbonil menjadi metilena.

Dimana
pada metode ini juga dibutuhkan kondisi basa yang sangat basa, reaksi ini tidak
dapat atau tidak cocok bagi substrat yang snsitif terhadap bassa.
Mekanisme
:

Mekanisme
ini melibatkan pembentukan hydrazon lewat kondensasi hidrazin dengan aldehid
ataupun keton sebagai substart. Dimana hidrazon terdeprotonasi oleh bassa
alkoksida diikuti pula degan tahap penentu laju reaksi, secara bersamaan suatu
anion diimida terbentuk. Kemudian rusaknya alkildimida ini dengan lepasnya N2
dan ini menjarah pada pembentukan alkil anion yang diprotonasi oleh pelarut dan
membentuk produk yang diinginkan.
Kemudian
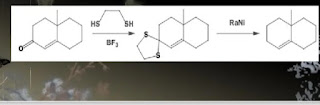
Metode Mozingo
Dimana
pada prinsipnya mengubah gugus
karbonil menjadi tioasetal, yang selanjutnya direduksi oleh nikel Raney.

Dimana ia melepaskan
gugus karbonil aldehid dan keton dengan menjadikannya tioasetal. Dan disini Ikatan
C-O merupakan ikatan yang kuat, dan ikatan C-S lebih lemah, dan mudah direduksi
dengan Nikel Raney.
Metode
Clemmensen
Reaksi
ini ditokohi oleh seorang ilmuan asal Denmark yaitu Erik Christian Clemmensen.
Ini adalah suatu reaksi kimia dengan reduksi aldehid aatau keton menjadi alkana
menggunakan amalgam seng dan asam.

Pada
Mekanisme 1:

·
oksigen
dari gugus karbonil terprotonasi oleh asam
·
Ikatan
seng-karbena kemudian terbentuk saat transfer elektron terjadi.
·
Setelah
protonasi yang diperbaharui dan transfer elektron, molekul air memisahkan diri
dan kompleks seng-karbon yang terbentuk.
·
Hidrokarbon dibebaskan melalui tahap protonasi sebanyak dua
kali dan dengan transfer elektron sebanyak dua kali.

Pada mekanisme 2
·
Sebuah elektron ditransfer pada karbon karbonil
·
Akibatnya, ikatan oksigen-seng terbentuk dan
pada saat yang bersamaan anion karbon-radikal terbentuk.
·
Oksigen ditransfer pada seng dengan cara transfer elektron ganda dan karbena
karbon-seng terbentuk. Hidrokarbon kemudian
dilepaskan seperti dijelaskan pada mekanisme 1, melalui protonasi dan transfer elektron.
Ø Menjadi Alkohol
Pada reduksi aldehid dan keton menjadi alkohol, tterbagi
menjadi dua berdsarkan jenis agen pereduksinya, yaitu pereaksi transfer hidrida
dan transfer elektron. Untuk pereaksi transfer hidrida, terdapat tiga jenis
reaksi, yaitu dengan pereaksi logam hidrida, reaksi Cannizaro dan
reaksi Meerwein–Ponndorf–Verley.
1.
Pereaksi
logam hidrida
Pada
pereaksi logam hidrida ada dua macam jenis agennya yaitu natrium borohidrida
(NaBH4) dan litium aluminium hidrida (LiAIH4)

Borohidrida
mentransfer hydrogen dengan pasangan elektron ikatannya ke karbon parsial
positif pada gugus karbonil. Oksigen yang parsial negatif menyerang boron.
Selanjutnya, semua hydrogen pada borohidrida ditransfer dan terbentuk
tetraalkoksiborat.

Hidrolisis atau alkoholisis mengkonversi
intermediate tetraalkoksiborat menjadi alkohol.
Litium Aluminium Hidrida

Penambahan air mengkonversi tetra alkoksi
aluminat menjadi alkohol
·
Reaksi Cannizaro
Reaksi
aldehid dan keton yang tidak mengandung atom hydrogen α dengan basa akan
menghasilkan suatu alkohol dan juga asam karboksilat.
Adapun mekanismenya ialah

Tahap A

Tahap B

·
Reaksi Cannizaro
Reduksi keton menjadi alkohol menggunakan Al(Oi-Pr)3 dalam isopropanol.
Adapun mekanismenya ialah

Pereaksi Transfer elektron, merupakan suatu logam yang
dapat dengan mudah memberikan elektronnya. Logam mentransfer satu elektron ke
gugus karbonil untuk membentuk radikal anion. Senyawa ini diprotonosi dan
elektron yang kedua ditransfer untuk menghasilkan ion alkoksida.
Dikatakan bahwa Ikatan C-O merupakan ikatan
yang kuat, dan ikatan C-S lebih lemah, dan mudah direduksi dengan Nikel Raney, mengapa demikian?
2. Mengaapa pada metode Wolff-Kishner
dimana pada metode ini mengubah gugus fungsional karbonil menjadi metilena.
Dimana pada metode ini juga
dibutuhkan kondisi basa yang sangat basa, dan dikatakan reaksi ini ttidak cocok
bagi substrat yang snsitif terhadap bassa. Mengapa demikian?
Saat Hidrokarbon dibebaskan melalui tahap protonasi, mengapa sebanyak
dua kali dan dengatransfer elektron sebanyak dua kali pula?



Baiklah saudari Halimah. Disini saya akan mencoba menjawab pertanyaan Anda nomor 1. Menurut referensi yang saya baca, disini saya mengambil referensi dengan membandingkan energi ikatan pada kedua jenis ikatan karbon tersebut. Ikatan C-C memiliki energi ikatan sebesar 348 kJ/mol . Sedangkan, ikatan C-S memiliki energi ikatan sebesar 259 kJ/mol. Energi ikatan C-S lebih rendah daripada energi ikatan C-C. Menurut saya, inilah alasan mengapa ikatan C-S lebih mudah direduksi oleh Ni-Raney karena lebih rendah energi ikatannya sehingga mudah untuk direduksi.
BalasHapusassalamualaikum halimah
BalasHapussaya yupita sri rizki,Nim:A1C118071
Akam mencoba menjawab permasalahan no 2
Karna menurut saya jika hidrokarbon di bebaskan melalui tahap protonasi sebanyak dua maka tranfer elektronnya juga harus dua kali,jika tranformasi elektron hanya terjadi sekali maka produk yang di hasilkan tidak akan sesuai dengan yang seharusnya.seperti pada Mekanisme 2 menyatakan bahwa sebuah elektron ditransfer pada karbon karbonil. Akibatnya, ikatan oksigen-seng terbentuk dan pada saat yang bersamaan anion karbon-radikal terbentuk. Oksigen ditransfer pada seng dengan cara transfer elektron ganda dan karbena karbon-seng terbentuk. Hidrokarbon kemudian dilepaskan seperti dijelaskan pada mekanisme 1, melalui protonasi dan transfer elektron.
2. WISLIANA (A1C118060)
BalasHapusDimana pada reaksi no 2 menggunakan metode Wolff Kishner ini membutuhkan kondisi basa yang sangat basa, dan dikatakan reaksi ini tidak cocok bagi substrat yang sensitif terhadap basa dikarenakan pada metode ini membutuhkan kondisi yang sangat basa oleh karena itu tidak cocok bagi substrat yang sensitif terhadap basa. Secara umum mekanisme reaksinya ialah melalui pembentukan hidrazon. Kemudian selanjutnya hidrazon terprotonasi oleh basa alkoksida. Dari penjelasan tersebut hidrazonnya terprotonasi oleh basa tersebut bisa kita ambil kesimpulan bahwa pada reaksi diatas membutuhkan kondisi yang sangat basa (substrat yang sensitif terhadap asam) tidak menggunakan substrat yang sensitif terhadap basa supaya hidrazonnya bisa terprotonasi.
Terima kasih